|
Syngas ou Gaz de synthèse
Production combinée de chaleur et délectricité
Le biométhane de 2ème génération
|
Publicité
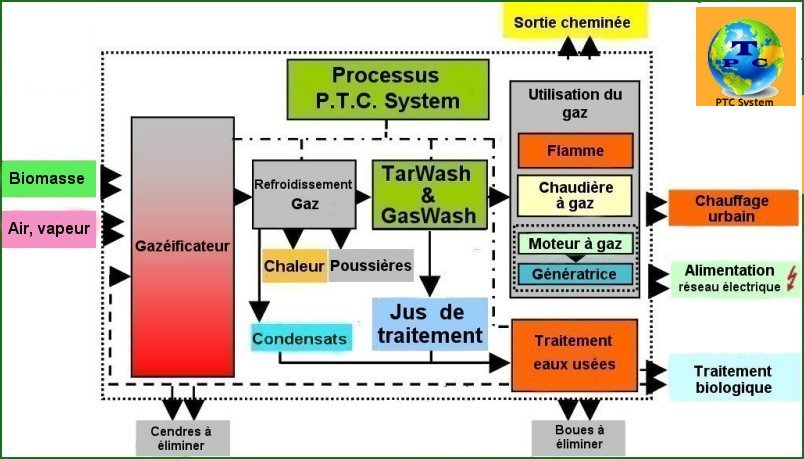
Syngas
P.T.C.
System et la purification du Syngaz de déchets
solides
La
« gazéification » désigne une transformation
thermochimique consistant à décomposer
par la chaleur un solide combustible carboné
(charbon, biomasse) en présence dun réactif
gazeux (gaz carbonique, vapeur deau puis
oxygène/air) dans le but dobtenir un
mélange gazeux combustible.
La réaction de gazéification se passe
dans des conditions de température très
élevées (plus de 1 000 °C).
Le gaz de synthèse obtenu à la fin, appelé
« syngas » (pour « synthetic gas »), est
un mélange de deux gaz combustibles :
Lle
monoxyde de carbone (CO) et lhydrogène
(H2).
Les
"Syngas" également appelés gaz de synthèse,
gaz synthétiques ou gaz de gazogène, peuvent être
produits à partir de différentes matières contenant
du carbone.
Elles incluent notamment la biomasse (gaz de bois),
les matières plastiques, le charbon, les déchets ménagers
ou matières similaires.
Un syngas est un mélange gazeux combustible produit
par pyrolyse. C'est un gaz pauvre et sale, toxique,
acide, et corrosif s'il n'a pas été soigneusement
épuré.
Historiquement, les gaz de ville étaient utilisés
pour alimenter de nombreuses résidences en Europe,
et dans dautres pays au cours du 20ème siècle.
Composition
moyenne du syngas:
|
Substance
|
Composition
(%)
|
|
Hydrogène
(H2)
|
20-40
|
|
Monoxyde
de carbone (CO)
|
35-40
|
|
Dioxyde
de carbone (CO2)
|
25-35
|
|
Méthane
(CH4)
|
0-15
|
|
Azote
(N2)
|
2-5
|
La
gazéification génère
de nombreux composés dont
on doit se débarrasser:
Goudrons, NOx, dioxines et furanes,
HCL, H2S, poussières, mercure...
Ainsi
les constituants du syngas à traiter
sont :
-
chlorure
dhydrogène (HCl),
-
-
le sulfure dhydrogène (H2S),
-
-
les
poussières polluants particulaires
(solides/carbone, liquides/aérosols,
),
-
-
les HAP (Hydrocarbures aromatiques
polycycliques),
-
les COV (Composés Organiques Volatils),
-
les composés bromés et iodés,
-
-
le
dioxyde de carbone (CO2),
-
les
inorganiques et les alcalins.
Le
tableau suivant présente les formes
sous lesquelles les constituants
sont présents en milieu réducteur,
comparés à celles en milieu oxydant
(incinérateur par exemple) :
|
Elément
|
Milieu
oxydant
|
Milieu
Réducteur
|
| Soufre
|
SOx |
H2S
(majoritaire), COS, CS2 |
| Azote |
NOx
|
N2,
HCN, NH3 |
| Chlore
|
HCl
|
HCl,
NaCl, KCl, PbCl2,
|
| Plomb |
PbO,
PbCl2 |
PbS,
PbCl2 |
| Mercure |
HgO,
HgCl2 |
Hg0
(majoritaire), HgCl2, HgS |
-
Techniques
dabattage au sein même du gazéifieur:
Des absorbeurs ou des catalyseurs
sont mélangés à la charge pour
traiter le H2S (ajout doxyde
de calcium) et les goudrons (par
réaction catalytique avec la vapeur
deau et le CO2).
-
Techniques
dabattage dans des équipements
connexes:
Filtration des poussières (cyclones
ou électrofiltres), lavage à leau
ou craquage catalytique à haute
température pour labattage des
goudrons, labattage du H2S par
absorption (lavage chimique ou
solvant), capture du HCL par lavage
à leau ou sur absorbant, captation
des métaux par charbon actifs
(mercure en particulier).
Un
verrou technologique commun aux syngas:
L'élimination des goudrons produits lors
de la pyrolyse de la biomasse (encrassements,
corrosion, désactivation des catalyseurs de
méthanation
)
Il existe un grand nombre de technologies
pour lélimination des goudrons. On rencontre
couramment des solutions de condensation et
dabsorption des goudrons au moyen dun solvant
organique par exemple ou des systèmes de traitement
à haute température tels que des craqueurs thermiques
ou des vaporeformeurs.
Le
syngas est utilisé principalement :
-
Comme
source de production de chaleur
-
Comme
source de production délectricité par laction
du gaz sur des turbines
-
Comme
source de production dhydrogène, de méthanol
et de méthane par traitement chimique
-
Comme
source de production de carburant de synthèse
par le procédé Fischer-Tropsch
-
Production d'énergie renouvelable
-
Conversion
des déchets problématiques en combustibles
utiles
-
Production
économique d'énergie sur le site et réduction
des pertes de transmission
-
Réduction
des émissions de carbone
Comment
produit-on le syngas ?
Plusieurs
réactions successives sont nécessaires. Lensemble
de ce processus est appelé gazéification.
Il nécessite, à partir dune matière organique,
dobtenir au préalable dans le réacteur de la
vapeur deau (H2O) et du carbone (C) et de produire
une chaleur suffisante pour la réaction finale
de gazéification.
Quatre étapes successives, fortement couplées,
sont nécessaires, la troisième produisant la
chaleur requise par les trois autres.
1ère
étape : séchage de la matière pour produire
de la vapeur deau
Cette étape se déroule à des températures comprises
entre 100°C et 160°C. Sous leffet de la chaleur,
leau contenue dans la matière organique sévapore.
Le combustible carboné résultant est sec et
de différentes natures (charbon, biomasse, etc.).
Dans le cas de produits non homogènes, une phase
préalable (tri, broyage) est nécessaire avant
dintroduire cet intrant dans le gazéifieur.
2ème
étape : pyrolyse des intrants pour obtenir du
coke (résidus de carbone) et des gaz de pyrolyse
Cette étape sans oxygène (anaérobie) se déroule
à des températures situées entre 120 °C et 600
°C. Elle est dite "autothermique"
car elle ne produit ni ne consomme dénergie.
En augmentant progressivement la température
en labsence doxygène, la matière séchée se
décompose et les atomes de carbone sassocient
entre eux.
Il se forme alors du carbone réducteur presque
pur (coke ou résidus de carbone) et un mélange
de gaz oxydants non-condensables composés majoritairement
doxyde de carbone (CO) et dhydrocarbures (CH4)
appelés "gaz de pyrolyse" ; des goudrons
et des matières volatiles condensables issues
de vapeurs de composés organiques (acides acétiques,
aldéhydes, etc...).
3ème étape : oxydation des gaz de
pyrolyse pour générer une chaleur suffisante
à la gazéification
Cette étape se déroule en présence doxygène
à des températures comprises entre 1 200°C et
1 500°C.
Les matières volatiles issues de la pyrolyse
soxydent. Cette combustion dégage la chaleur
nécessaire aux deux étapes précédentes et à
létape suivante de la gazéification. Elle nécessite
un fort apport en oxygène.
4ème
étape : la réduction ou « gazéification » du
carbone pour produire le syngas
Cette étape se déroule à des températures comprises
entre 800 °C et 1200° C. En labsence doxygène,
le coke obtenu lors de la phase de pyrolyse
réduit la vapeur deau et le gaz carbonique
obtenus dans létape précédente respectivement
en hydrogène et en oxyde de carbone pour former
du syngas, combustible d'un mélange en
proportions variables CO et H2.
Les
différents procédés de gazéification
Le
procédé à lit fixe, Il peut être soit à co-courant
soit à contre-courant.
Procédé
à co-courant
Les différentes étapes de la réaction de gazéification
sont successivement réalisées de haut en bas dans
le réacteur.
La matière organique est dabord introduite à
son sommet.
De lair est injecté à mi-hauteur pour amorcer
la combustion et fournir de la chaleur à lensemble
du réacteur.
Laugmentation progressive de la température permet
dobtenir les différentes réactions entraînant
les gaz produits vers la zone la plus chaude du
réacteur.
Le syngas est récupéré au niveau du socle du gazeifieur
Procédé
à contre-courant
Lair est injecté à la base du réacteur et le
syngas est récupéré sous son sommet, au dessus
de la zone de pyrolyse.
Les goudrons sont moins nombreux à séchapper
du réacteur et lencrassement des conduits est
donc plus limité.
-
Le
procédé à lit fluidisé statique.
Par ce procédé, les particules sont mises
en suspension dans le réacteur par injection
à sa base dun gaz qui va "soulever"
les grains.
Cela favorise les échanges thermiques et massiques
entre le gaz et le solide.
Dans ce type de réacteur, les différents mécanismes
de séchage, pyrolyse, combustion ou oxydation
ont lieu dans une seule et même zone.
-
Le
procédé à lit fluidisé entraîné.
Le solide combustible carboné est finement
pulvérisé dans un jet d'oxygène.
La réaction chimique seffectue à très haute
température et à pression élevée.
Cela empêche les goudrons et le méthane de
se former, les gaz produits en sont ainsi
exempts. Le rendement en gaz est donc élevé.
Cependant, le procédé à lit fluidisé entraîné
nécessite une forte consommation en oxygène.
Par ailleurs, le coût de la pulvérisation
préalable du solide combustible carboné est
élevé car il faut obtenir une biomasse ou
du charbon finement divisé.
Le
syngas à partir de la biomasse
La
biomasse peut être utilisée sous forme solide,
liquide ou gazeuse. La biomasse liquide correspond
aux effluents d'élevage valorisés par méthanisation
mais aussi aux biocarburants.
La biomasse gazeuse correspond au gaz de synthèse
(syngas) issu du bois.
Le
syngas de bois
On distingue deux grands types de ressources
en bois énergie : la ressource sylvicole et
la ressource industrielle. A noter que lorsque
l'on parle de bois énergie, il s'agit exclusivement
de bois "non traité".
Le
gisement des déchets de bois est estimé à 14
millions de tonnes en France.
Selon l'ADEME, 90% de ces déchets sont valorisés
et 49% font l'objet d'une valorisation matière.
On distingue traditionnellement trois sortes
de bois:
-
Les
bois de classe A (bois non traités), issus
des sous-produits de la transformation du
bois brut, bois secs non-traités et non
peints, palettes...
-
Les
bois de classe B (bois faiblement traités),qui
rassemblent les panneaux, les bois d'ameublement,
les bois de démolition exempts de gravats,
les résidus d'exploitation forestière (souches,
grumes etc.)
-
Les
bois de classe C traités à la créosote (traverses
de chemin de fer, poteaux téléphoniques...)
ou autoclavés et imprégnés de sels métalliques
(piquets de vigne et d'arboriculture, écrans
acoustiques, glissières de sécurité...)
nécessitent des équipements adaptés pour
leur élimination en raison notamment des
risques d'émission dans l'atmosphère de
divers composés organiques volatils polluants
(HAP...) et de métaux lourds : ils sont
détruits en usine d'incinération de déchets
spéciaux ou utilisés dans les fours de cimenteries.
-
La
ressource industrielle
La
ressource industrielle est la moins
importante mais la plus sollicitée,
elle peut se répartir en deux origines
:
-
Le
bois de rebut
Le
bois de rebut est constitué
de produits en fin de vie (bois
d'emballage, de déconstruction...)
Le gisement est disponible mais
sa valorisation est difficile
car celui-ci est diffus ce qui
rend la collecte difficile et
aussi parce quil peut contenir
des corps métalliques, plastiques
ou des souillures.
-
Les
sous-produits des industries du bois
Lindustrie
de première transformation produit lessentiel
des sous-produits industriels sous forme
décorces ou de sciures. Le rendement matière
des industries de la seconde transformation
du bois étant bien supérieur à celui des
scieries, le gisement potentiel en chutes
est bien plus faible, dautant que lassociation
du bois à dautres matériaux rend impossible
leur valorisation en centrale thermique.
Avec un taux dhumidité de 40 à 60 %, la
principale valorisation des écorces est
la combustion en chaudière de forte capacité
(> 1 MW).
Quant aux sciures de bois, elles ont une
humidité équivalente à celle du bois scié
(50 à 70 %).
Le
bois étant une des ressources principale de
la biomasse solide, il occupe une place importante
dans la filière.
Les
différents combustibles bois
-
La
bûche
est
la
forme
la
plus
commune
du
bois
et
celle
qui
subit
le
moins
de
transformations.
Elle
est
utilisée
en
majeure
partie
par
les
particuliers
dans
des
inserts
ou
des
foyers
fermés,
des
poêles
et
des
chaudières
manuelles.
Afin
de
garantir
une
efficacité
maximale,
le
taux
dhumidité
de
la
bûche
doit
être
inférieur
à
22
%.
-
Le
granulé
Le
granulé
de
bois
résulte
de
la
compression
de
sciures
propres
issue
généralement
des
scieries.
Le
granulé
est
un
combustible
normé.
-
Le
bois
déchiqueté
Le
bois
déchiqueté
(sous
forme
de
plaquettes
de
quelques
centimètres
de
longueur)
a
plusieurs
origines:
-
Sous-produit
de lexploitation
forestière et
arboricole (branches,
houppiers, rémanents
);
-
Sous-produit
non souillés
des industries
du bois (scieries,
emballages, palettes,
cagettes, etc.).
Le
syngas de déchets solides
La
gazeification des déchets industriels ou ménagers
dans une enceinte de traitement en défaut dair
et enrichie en vapeur deau et dioxyde de carbone
(agents réactionnels), les matières volatiles
émises ne subiront pas de processus de combustion.
Le carbone fixe se mettra à réagir avec la vapeur
deau et le CO2, à des températures de 850-900°C,
dans des réactions endothermiques de transformation
thermochimiques, dites de gazéification, de
type schématique:
| C
+ H2O —> CO + H2 (pyrolyse) |
C
+ CO —> 2CO (gazéification) |
C
+ H2 —> CH4 (méthanation) |
Les
deux premières réactions sont favorisées à haute
température (850-900°C) et basse pression (~
1 bar), tandis que la dernière est favorisée
à basse température (700°C) et haute pression
(10-20 bars).
Les
déchets solides sont de provenances diverses
-
-
DIB
(Déchet industriel banal),
-
RBA
(Résidus de broyage automobile),
-
-
Boues
de stations d'épuration etc...
Syngas
et Biométhane de 2ème génération
Le
biométhane de 2ème génération
sera produit à partir de biomasse ligno-cellulosique
(bois et paille) par un procédé appelé conversion
thermochimique comprenant une étape de gazéification
puis une étape de méthanation.
La
gazéification aboutit à lobtention dun gaz
pauvre en méthane et constitué dun mélange
deau, de monoxyde de carbone (CO) et de dioxyde
de carbone (CO2). La méthanation permettra
d'enrichir ce syngas.
Le
processus serait une réduction du CO
et du CO2 par H2 déjà présent
lors de la fabrication d'un syngas.
Chauffée
entre 800 et 1.000 degrés, la biomasse produit
le syngas dont les atomes de carbone, d'oxygène
et d'hydrogène obtenus sont recombinés par le
biais de catalyseurs pour former un biogaz à
une très haute quantité de méthane (>97%).
la gazéification suivie de la méthanation de
la biomasse n'étant pas encore maîtrisées technologiquement,
ce processus est à l'état de recherche & développement.
La biomasse utilisée étant plus ligneuse et
moins humide que celle pour la méthanisation,
le biocarburant obtenu possédera un rendement
énergétique plus élevé.
Ce nouveau biométhane permettra de traiter
une fraction de coproduits issus de diverses
industries et filières (bois de construction,
coproduits des industries agroalimentaires,
boues de station dépuration,
).
Forte du patrimoine forestier et agricole français,
la filière biométhane de gazéification posséderai
un potentiel de plus de 100 TWh/an à horizon
2020 et de plus de 250 TWh/an à horizon 2050.
La
méthanation au service des énergies renouvelables
Méthanisation
et méthanation sont deux technologies bien distinctes.
-
La
méthanisation est un procédé industriel qui
tire parti de la dégradation de matière organique
(plus précisément de la fermentation anaérobie)
afin de produire du biogaz. Ce biogaz peut
par la suite être utilisé dans la production
de chaleur ou délectricité. Cette technologie
est déjà largement exploitée et devrait dailleurs
se développer davantage puisquelle a un
réel rôle à jouer dans la transition énergétique.
-
La méthanation, quant à elle, a une tout autre
vocation. En effet, elle pourrait permettre
le stockage de lénergie.
Comme on le voyait dans un précédent article,
le stockage à grande échelle de lénergie
est nécessaire afin dopérer la transition
énergétique vers un mix davantage décarboné.
Quil sagisse de stocker lénergie produite
par les EnR afin de la restituer en consommation
de pointe ou bien de stocker lénergie nucléaire
quand nous sommes en surproduction, cette
solution nous promet des rendements importants
et une méthode fiable.
Il
sagit dabord de produire de lhydrogène puis
de faire réagir cet hydrogène avec du dioxyde
de carbone dans un réacteur "catalytique".
Les deux piliers de cette production dénergie
sont donc dobtenir lhydrogène, et la méthanation
catalytique de lhydrogène et du dioxyde de
carbone qui aboutit à la production de méthane.
Nous devons dailleurs cette découverte à un
chimiste français, Paul Sabatier, qui formalisa
il y plus dun siècle les conditions nécessaires
à la production de méthane à partir de la réaction
du lhydrogène et du dioxyde de carbone.
Ce procédé est exploité depuis de nombreuses
années dans le secteur de la chimie ou par la
NASA pour produire de leau sur la station internationale.
Des
projets français comme ElectroHgena, piloté
par Areva, proposent, grâce à des améliorations
technologiques, des rendements de lordre de
75%.
La méthanation a pour avantage de considérer
le gaz carbonique comme une ressource plutôt
que comme une contrainte, et permet ainsi de
valoriser le C02 en se positionnant comme une
énergie non génératrice directe de gaz à effet
de serre.
Bien quelle ne permette pas de stocker le CO2
cette solution offre en revanche de récupérer
une énergie qui aurait habituellement été perdu,
celle des EnR quand la production nest pas
adaptée à la demande, et celle des centrales
nucléaires.
|
|
![]() Valorisation
Valorisation